
Садржај
У овом чланку: Употреба пХ мерача Употреба сунцокретовог папираУкључивање пХ8 референце
Важно је анализирати пХ воде (тј. Ниво киселости или лужине). Воду конзумирају биљке и животиње од којих овисимо и конзумирамо је директно сваког дана. ПХ воде може дати трагове потенцијалној контаминацији. Стога је анализа пХ воде важна мјера јавног здравља.
фазе
Метода 1 Коришћење пХ метра
-

Калибрирајте сонду и мерач према упутствима произвођача. Да бисте га калибрирали, можда ћете морати да тестирате мерач са познатом пХ супстанцом. Затим можете да га подесите на основу ових мерења. Ако ћете анализирати воду изван лабораторија, извршите калибрацију пре него што оштетите уређај на терену.- Испрати сонду пре употребе чистом водом. Осушите га чистом крпом.
-

Сакупите узорак воде у чисту посуду.- Узорак воде треба да буде довољно дубок да врх електроде буде покривен.
- Оставите узорак неко вријеме да се одмори тако да се температура стабилизира.
- Измерите температуру узорка термометром.
-

Подесите мерач у складу са температуром узорка. На осетљивост сонде утиче температура воде и назначено мерење можда неће бити добро ако не унесете температурне податке. -

Ставите сонду у узорак. Сачекајте да се мерач уравнотежи. Ово се постиже када мерење остане стабилно. -

Прочитајте мерење пХ узорка. Ваш пХ мерач треба да вам мери на скали од 0-14. Ако је вода чиста, мјерење треба бити близу 7. Запишите своје записе.
2. метод Користите сунцокретов папир
-

Научите разлику између пХ папира и сунцокретовог папира. Да бисте добили тачно мерење раствора, можете користити пХ папир. Не треба мешати са тренутним папиром од сунцокрета. Обе се могу користити за анализу киселина и база, али се радикално разликују.- Траке пХ садрже низ индикаторских стубова који мењају боју након излагања раствору. Интензитет киселина и база сваке колоне се разликује. Једном када се промене, боје се могу упоредити са примерима који се дају у комплету.
- Сунцокретов папир састоји се од папирних трака које садрже киселину или базу (алкалну). Већину времена су црвене (ако садрже киселину која реагује са базама) или плаве (ако садрже базу која реагује са киселинама). Црвене траке постају плаве ако је супстанца алкална, плаве траке постају црвене ако су у контакту са киселином.Сунцокретови папири се могу користити за брзо и лако мерење, али јефтинији не морају нужно да тачно мере пХ вредности раствора.
-

Сакупите узорак воде у чисту посуду. Узорак треба да буде довољно дубок да се трака може прекрити. -

Умочите трак папира у свој узорак. Неколико секунди излагања би требало бити довољно. Различите колумне папира почеће да мењају боју за неколико тренутака. -

Упоредите крај траке за анализу са обојеним графиконом који је приложен уз папир. Боје на графикону треба да се подударају са бојама на вашем бенду. Свака боја треба да буде повезана са мерењем пХ.
Метода 3 Разумевање пХ
-
Откријте како су дефинисане киселине и базе. Лакоћа и алкалност (појам који се користи за описивање база) су обе дефинисани водоничним јонима које губе или прихватају. Киселина је супстанца која губи (или према неким даје) водоничне јоне. -
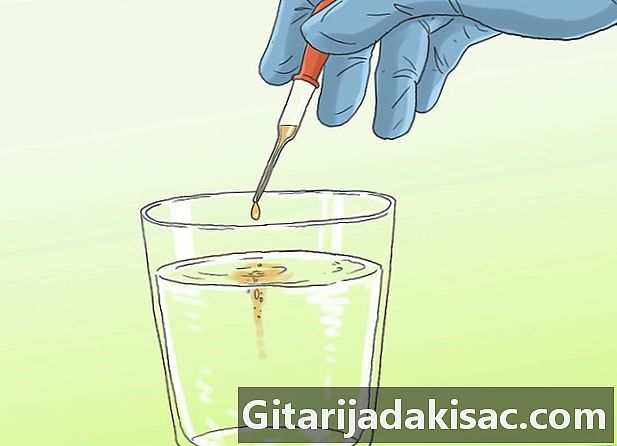
Разумевање скале пХ. ПХ број користи се за процену нивоа киселости или алкалности материја растворљивих у води. Вода обично садржи еквивалентни број хидроксидних (ОХ-) и хидронијумских (Х30 +) јона. Када се у воду дода кисела или алкална супстанца, она мења пропорцију хидроксидних и хидронијум јона.- Овај број је обично на скали од 0 до 14 (мада неке супстанце могу заправо превазићи овај опсег). Неутралне материје имају пХ близу 7, киселе материје испод 7 и алкалне супстанце изнад 7.
- ПХ-скала је логаритамска, што значи да је разлика од једне јединице заправо 10 пута већа разлика у киселости или лужини. На пример, супстанца са пХ 2 је заправо 10 пута киселија од материје чији је пХ 3 и 100 пута киселији од супстанце са пХ пХ 4. Вага делује на исти начин и за алкалне материје, мерна јединица која одговара десетострукој разлици.
-

Знајте зашто желимо да измеримо пХ воде. Чиста вода треба да има пХ од 7, али вода из славине обично има пХ између 5,5 и 6. Високо кисела вода (са ниским пХ) је вероватнија да раствара токсичне производе. Они могу контаминирати воду и учинити је непримереном за људску употребу.- Уопште је пожељно мерење пХ ин ситу. Ако прикупите узорак воде за проучавање у лабораторији, угљендиоксид у води може да се растопи у води. Овај растворени угљен диоксид реагује са јонима који су присутни у води и повећава киселост основних или неутралних раствора. Да бисте избегли загађење угљен-диоксидом, требало би да измерите воду мање од 2 сата након што сте је сакупили.